Marker für Beweglichkeit von Krebszellen
Neuer Marker liefert gute Vorhersagbarkeit für das Auftreten von Metastasen.
Wissenschaftler unter Federführung der Universität Leipzig haben eine wegweisende Anwendung der „Physik des Krebses“ in der Onkologie gefunden. Dies markiert einen Meilenstein für das neue wissenschaftliche Gebiet, das erstmals deren Anwendbarkeit in der Medizin belegt. Basierend auf Gewebe- und Zellmechanik sowie dem Einsatz von maschinellem Lernen haben sie einen Marker für die Beweglichkeit (Motilität) von Krebszellen in der digitalen Pathologie entwickelt. Die neue Information über Brusttumore, die der Marker liefert, verbessert die die Vorhersage des Riskos für das Auftreten von Metastasen selbst nach einem Jahrzehnt.
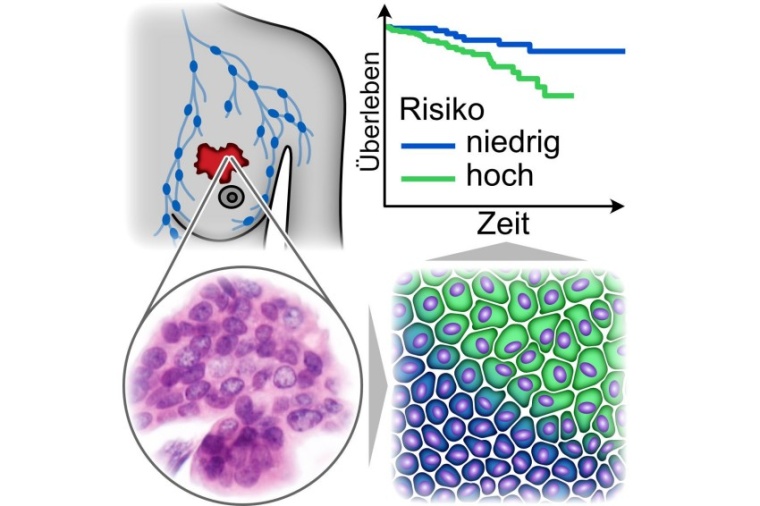
In einer retrospektiven Studie mit 1380 Brustkrebspatientinnen, die in enger Zusammenarbeit mit Axel Niendorf von der Pathologie Hamburg-West entstand, fand der Doktorand Pablo Gottheil aus der Arbeitsgruppe von Josef Alfons Käs von der Universität Leipzig heraus, dass ein gemeinsamer Übergang der Krebszellen zur Beweglichkeit, bekannt als „Unjamming“, das Risiko für Fernmetastasen signifikant erhöht. Fernmetastasen entstehen, wenn die Krebszellen andere Organe befallen. „Dieser Prozess spielt eine entscheidende Rolle bei der Krebsaggressivität und könnte ein wichtiger zusätzlicher Prognosefaktor für das Streuungsrisiko eines Tumors sein“, sagt Josef Alfons Käs, Leiter der Abteilung für Physik weicher Materie an der Universität Leipzig.
Im Primärtumor bilden die Krebszellen Cluster, in denen sie dichtgedrängt sind, so dass sie sich gegenseitig einklemmen („Jamming“) und sich nicht bewegen können. Im Verlauf des Tumorwachstums kommt es zu einem kollektiven Beweglichkeitsübergang, wodurch die Krebszellen den Tumor verlassen und streuen können. Dabei nehmen die Krebszellen eine längliche Form an, die es ihnen ermöglicht, sich aneinander vorbeizudrücken. Die in der Diagnose von Brustkrebs verwendeten histologischen Tumorschnitte sind statische Bilder, in denen die Zellbewegung nicht verfolgt werden kann. „Nun haben wir erkannt, dass wir anhand länglicher Form und geringerer Dichte bewegliche Krebszellen in diesen histologischen Bildern identifizieren können. Wir haben also einen ersten Marker entwickelt, der es ermöglicht, bewegliche Krebszellen, die sich ausbreiten und deshalb streuen können, in histologischen Tumorschnitten zu erkennen. Wir konnten zeigen, dass eine hohe Anzahl solcher beweglichen Zellen in einer Tumorprobe das Risiko einer Metastasierung deutlich erhöht“, erläutert Biophysiker Käs.
„Die Brustkrebstherapien könnten erheblich verbessert werden, wenn eine präzisere Diagnose möglich wäre. Es gibt viele verschiedene, differenzierte Behandlungsansätze. Da allerdings die momentane Diagnose nicht genau vorhersagen kann, wie die Krankheit voranschreiten kann, kommt es zur Über- und Unterbehandlung der Patientinnen“, erklärt Käs. Ein wesentlicher Aspekt der Prognose bestehe darin, vorherzusagen, ob sich Metastasen im Körper bilden werden. Das derzeitige Hauptkriterium zur Beurteilung des Risikos der Metastasierung, also das Streuen des Krebses, ist der Befall der Lymphknoten in der Nähe des Tumors. Bei dieser Risikovorhersage verbleibt jedoch eine deutliche Fehlerquote. Etwa dreißig Prozent der Frauen mit befallen Lymphknoten entwickeln keine Fernmetastasen, während bei dreißig Prozent der Frauen ohne befallene Lymphknoten der Tumor streut.
Der von Käs und seinen Kollegen entwickelte, neue prognostische Marker hat laut der zugrunde liegenden Studie eine klinisch relevante Vorhersagekraft, die vergleichbar ist mit dem bisher in der Diagnostik angewandten Lymphknotenstatus. Dabei seien die beiden diagnostischen Kriterien in ihrer Vorhersagekraft komplementär und korrigierten so gegenseitig ihre Fehlvorhersagen. Dadurch bestehe die Möglichkeit, dass weniger Frauen über- oder untertherapiert werden. Vor allem erlaube der neue Marker eine frühere Prognose, da er bereits eine Vorhersage machen kann, bevor die Krebszellen den Tumor verlassen haben. Damit könne auch für Patientinnen in einem frühen Krankheitsstadium eine Prognose abgegeben werden, bei denen der Lymphknotenstatus noch nicht greift. Deshalb könnte der neue Ansatz der Forscher gerade bei der frühen Identifizierung besonders aggressiver Tumore relevant sein.
Diese Ergebnisse konnten nur durch die enge Zusammenarbeit mit Medizinern gewonnen werden. Ohne die große Anzahl von digitalen histologischen Schnitten von Brusttumoren, die von Niendorf zur Verfügung gestellt wurden, hätte die Studie Käs zufolge nicht durchgeführt werden können. Die Klinik für Frauenheilkunde am Universitätsklinikum Leipzig unter der Leitung von Bahriye Aktas stellte vitale Brusttumor-Explantate zur Verfügung. Damit konnten die Biophysiker bestätigen, dass die morphologischen „Unjamming“-Kriterien tatsächlich auf bewegliche Krebszellen zutreffen. Markus Löffler vom Institut für medizinische Informatik, Statistik und Epidemiologie der Universität Leipzig und sein Team unterstützten das Projekt mit der klinischen Auswertung und Interpretation.
Da sich das Verfahren nicht auf spezifische Moleküle im Tumor verlässt, könnte es auch bei anderen Tumortypen angewendet werden. Es besteht nach Ansicht der Forscher somit die Möglichkeit, das Verfahren bei 92 Prozent aller Krebspatientinnen anzuwenden. Mit weltweit über zwei Millionen Erkrankungen jährlich ist Brustkrebs die mit Abstand häufigste Krebserkrankung bei Frauen. Im Jahr 2018 starben mehr als 600.000 Frauen mit Brustkrebs, vor allem aufgrund der systemischen, invasiven Natur der Krankheit.
U. Leipzig / DE











