Smartes Pflaster aus dem 3D-Drucker
Grünes LED-Licht aktiviert heilende Proteine.
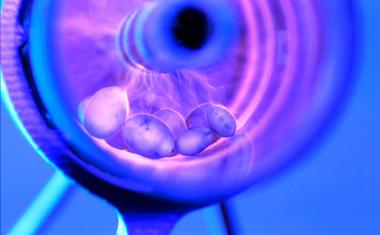
Durchblutungsstörungen, eine Diabetes-Erkrankung oder langes Liegen auf derselben Stelle können zu chronischen Wunden führen, die auch nach Wochen nicht abheilen. Wirkungsvolle Behandlungsmöglichkeiten gibt es kaum. Ein Forschungsteam aus den Materialwissenschaften der Christian-Albrechts-Universität zu Kiel hat zusammen mit Kolleginnen und Kollegen des Universitätsklinikums Schleswig-Holstein, der Harvard Medical School und der Dankook University, Südkorea, ein Wundpflaster mit heilungsfördernden Funktionen entwickelt, die patientenspezifisch angepasst werden können. Das per 3D-Druck hergestellte Pflaster wirkt antibakteriell, versorgt die Wunde mit Sauerstoff sowie Feuchtigkeit und unterstützt die Bildung von neuem Gewebe. Durch die Bestrahlung mit Licht wird die Wirkung aktiviert und gesteuert.

Basis des neu entwickelten Pflasters ist ein medizinisches Hydrogel. Durch seinen hohen Wassergehalt von neunzig Prozent und vergleichsweise großen Zwischenräumen auf der Mikroskala kann das Pflaster chronische trockene Wunden optimal versorgen. Wichtigster Bestandteil sind jedoch antibakteriell wirkende Zinkoxid-Mikropartikel, die auf Licht reagieren und von den Kieler Materialforschenden entwickelt wurden. Gemeinsam mit einem Team des Brigham and Women’s Hospitals der Harvard Medical School fanden sie einen Weg, um auf den Mikropartikeln spezielle Proteine aufzubringen. Mit zellschonendem grünem Licht werden die Proteine aktiviert und regen so die Bildung neuer Blutgefäße an. Durch die verbesserte Durchblutung entsteht neues Gewebe und die Wunde kann sich schließen.
„Indem wir die Wirkung des Pflasters mit Licht steuern, können wir den Verlauf und die Dosierung der Therapie an die individuellen Bedürfnisse von Patientinnen und Patienten anpassen“, sagt Rainer Adelung vom Institut für Materialwissenschaft. Das Material reagiert selbstständig auf äußere Reize und kann darüber kontrolliert werden. Ähnlich funktionierende Hydrogelpflaster, die ebenfalls gezielt aktiviert werden können, existieren bereits – sie entfalten ihre therapeutische Wirkung allerdings durch Wärme oder elektrische Signale. „Diese Konzepte haben jedoch den Nachteil, dass sich dabei auch die Wunde erwärmt und Hydrogele sich zu zersetzen beginnen“, erklärt Adelung.
Das Forschungsteam hofft, dass Kliniken sein multifunktionales, steuerbares Pflaster langfristig selbst im 3D-Drucker herstellen und mit sehr hellen, grünen LEDs direkt an den Patientinnen und Patienten aktivieren können. „Per 3D-Druck lässt sich sowohl die Form des Pflasters als auch die Konzentration der Zinkoxidpartikel und die Proteinsorte individuell anpassen“, sagt Leonard Siebert, der an der CAU gerade seine Promotion zu innovativen 3D-Druck-Methoden abgeschlossen hat. Während eines mehrmonatigen Forschungsaufenthalts an der renommierten Harvard Medical School in Boston arbeitete der Materialwissenschaftler in der Arbeitsgruppe von Su Ryon Shin, die medizinische Hydrogele mit speziellen Bio-3D-Druckern herstellt. „Unsere Partikel haben eine Tetrapodenform, sie bestehen also aus mehreren Armen. Dadurch lassen sich zwar besonders viele unserer wichtigen Proteine auf ihnen anbringen, aber sie passen nicht durch herkömmliche Druckerdüsen“, beschreibt Siebert eine der Herausforderungen ihres Ansatzes. In Boston entwickelte er schließlich eine Methode, um die Zinkoxidpartikel aus seiner Kieler Arbeitsgruppe zusammen mit den Hydrogelen zu drucken.
Außerdem arbeiteten die Kieler Forscher eng mit Helmut Fickenscher, Infektionsmediziner an der Uni Kiel und am Universitätsklinikum Schleswig-Holstein, zusammen. Er und sein Team testeten die antibakterielle Wirkung des Pflasters: Für 72 Stunden legten sie es auf einen Bakterienteppich und stellten fest, dass sich die Bakterien in einem Umkreis von mehreren Millimetern um das Pflaster nicht weiter ausbreiten. „Hierfür haben wir zwei typische Wundkeime verwendet, die sich in ihrem Aufbau grundlegend unterscheiden: Staphylococcus aureus und Pseudomonas aeruginosa. Das Pflaster zeigte bei beiden Grundtypen eine therapeutische Wirkung, was auf einen universalen Effekt schließen lässt”, fasst Gregor Maschkowitz, medizinischer Fachmikrobiologe am UKSH zusammen. Weitere Tests an Lebendmodellen wurden am NBM Global Research Center for Regenerative Medicine der Dankook University, Südkorea, durchgeführt. Erste Ergebnisse weisen auch hier auf eine gute Verträglichkeit des Pflasters und eine verbessere Wundheilung hin.
„Dieses Pflaster ist ein spannendes Konzept für die personalisierte Medizin, um Menschen mit auf sie zugeschnittenen Therapien möglichst gezielt, effektiv und schonend zu behandeln. Es ist ein konkretes Beispiel für das vielversprechende Potential der Zusammenarbeit von Medizin und Materialwissenschaft, die künftig immer wichtiger werden wird“, sagt Fickenscher. Nachdem die ersten Tests gezeigt haben, dass ihr Konzept grundsätzlich gut funktioniert, wollen die Forschenden jetzt die Steuerung per Licht noch weiter verbessern, um Patientinnen und Patienten künftig eine effektivere personalisierte Wundbehandlung anbieten zu können.
CAU Kiel / JOL
Weitere Infos
- Originalveröffentlichung
L. Siebert et al.: Light-Controlled Growth Factors Release on Tetrapodal ZnO-Incorporated 3D-Printed Hydrogels for Developing Smart Wound Scaffold, Adv. Func. Mat. 31, 2007555 (2021); DOI: 10.1002/adfm.202007555 - KiNSIS – Kiel Nano, Surface and Interface Science, Christian-Albrechts-Universität, Kiel