Diffraktion mit holographischer Referenz
Abbildung kleiner Biomoleküle lässt sich mit neuer Methode deutlich verbessern.
Single Particle Imaging (SPI) ist eine Methode, die Biomoleküle und ähnliche Teilchen mithilfe von superhellen Röntgenblitzen abbildet – wie zum Beispiel den Lichtblitzen, die von X-ray Free Electron Lasern erzeugt werden. Nun hat Forschungsgruppenleiter Kartik Ayyer am Max-Planck-Institut für Struktur und Dynamik der Materie in Hamburg einen neuen Ansatz für die hochaufgelöste Abbildung kleiner Biomoleküle entwickelt.
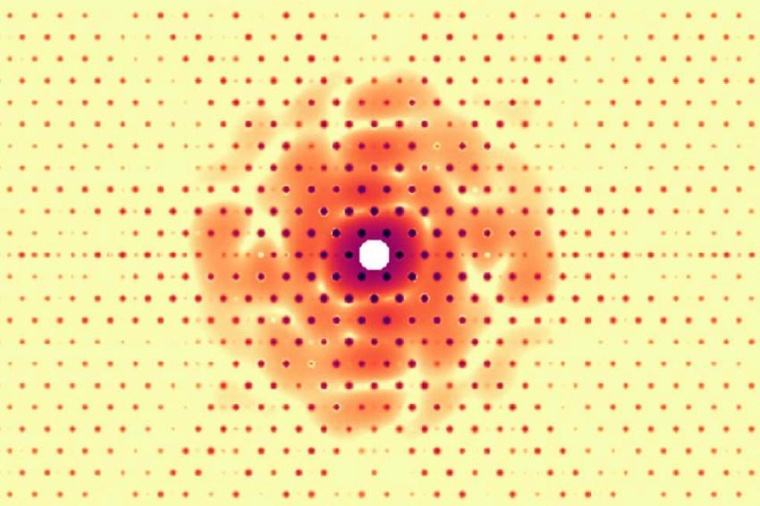
Wenn ein Laserstrahl auf das ein Molekül oder einen Kristall geschossen wird, erzeugt jedes Objekt ein Beugungsmuster, mit dem Wissenschaftler die Struktur und das Verhalten jenes Materials beschreiben. Die Forscher sammeln eine große Anzahl von Beugungsmustern von zufällig gedrehten Versionen dieser Partikel und kombinieren diese Informationen dann rechnerisch zu einer 3D-Struktur.
Kartik Ayyers Methode basiert darauf, dass bestimmte Materialien mit dem zu untersuchenden Teilchen kombiniert werden – entweder Goldnanopartikel oder 2D-Kristalle. Dadurch entsteht eine holographische Referenz, eine zusätzliche Beugung, die – paradoxerweise – das Beugungsmuster des zu untersuchenden Materials verbessert.
Holographische Referenzen können die Effizienz von SPI-Experimenten deutlich zu verbessern. Eine holographische Referenz befindet sich in unmittelbarer Nähe des Zielteilchens. Ihre Beugung interferiert mit der des Teilchens. Diese Interferenz hat den Vorteil, das Signal-Rausch-Verhältnis (SNR) zu verbessern, aber noch wichtiger ist, dass sie das Gesamtsignal deutlich erhöht. Dadurch werden die großen Probleme der Partikelerkennung und der Hintergrundtoleranz gemildert, die das Verfahren vor allem bei kleineren Objekten plagen.
Das Hauptproblem bei solchen Referenzen ist jedoch, dass das zusammengesetzte Objekt (Zielpartikel plus Referenz) in der Regel sehr heterogen ist. Dies bedeutet, dass sich mehrere Beugungsmuster kaum zu einer guten 3D-Struktur kombinieren lassen. Während die Idee der Holographie also mindestens seit den 1940er Jahren besteht (Dennis Gabor erhielt 1971 den Nobelpreis für die Methode) und seit Mitte der 2000er Jahre im SPI-Kontext vorgeschlagen wurde, konnte bisher noch niemand mit ihr hochaufgelöste 3D-Strukturen erzielen.
Ayyer, der Leiter der Computational Nanoscale Imaging-Gruppe am MPSD, hat einen neuen Algorithmus entwickelt, um die Struktur des Zielpartikels aus diesen zusammengesetzten Beugungsmustern zu rekonstruieren, indem er gleichzeitig die relativen Positionen, die Größe und andere Parameter der Referenz löst. Er schlägt zudem zwei experimentelle Konfigurationen vor, bei denen solche Referenzen verwendet werden könnten.
Die erste besteht darin, ein Gold-Nanopartikel auf dem Zielobjekt anzubringen und die Partikel in einem aerosolisierten Zustand abzubilden. Die experimentellen Methoden, sowohl für die Aerosol-Röntgenbildgebung als auch für das Anbringungsverfahren, haben sich in den letzten Jahren rasch entwickelt. Die zweite Konfiguration verwendet einen 2D-Kristall als Referenz. Das Signal wird nun in kristallographischen Spitzen konzentriert, was aus einer SNR-Perspektive ein wesentlicher Vorteil ist – die relative Position und Orientierung des Zielteilchens in Bezug auf die Einheitszelle des Kristalls muss jedoch für jedes Muster bestimmt werden.
„Diese Methoden sollten es uns ermöglichen, die SPI-Technik nicht nur auf große Viren und Proteinkomplexe auszudehnen, sondern auch auf wesentlich kleinere Partikel, die die Mehrheit der biologisch interessanten Moleküle ausmachen“, sagt Kartik Ayyer. „Genau wieviel kleiner diese sein könnten, werden wir mit den Simulationen herausfinden, die wir derzeit durchführen.“
MPSD / DE











