Entstehung des Lebens: Harnstoff-Umwandlung per Protonen-Tausch
Mit einer speziellen Röntgenquelle gelang die Enträtselung die ersten, schnell ablaufenden Schritte der lichtinduzierten Harnstoff-Umwandlung.
Wie begann das Leben auf der Erde? Eine der Hypothesen geht davon aus, dass die Ursprünge vor vier Milliarden in warmen Pfützen zu suchen sind. Das Wasser darin hatte vermutlich Harnstoffmoleküle enthalten. Dieser war der UV-Strahlung der Sonne ausgesetzt, die damals weitgehend ungehindert zur Erdoberfläche durchdringen konnte. Das energiereiche Licht vermochte den Harnstoff – Kohlensäurediamid – umzuwandeln. Aus den Reaktionsprodukten konnten sich dann Biomoleküle bilden, die später als Bausteine des Lebens fungierten. Diese „Warme-Pfützen“-Theorie war einer der Beweggründe für ein neuartiges Experiment, konzipiert von einem deutsch-schweizer Forschungsteam unter Leitung von Hans Jakob Wörner von der ETH Zürich und Jean-Pierre Wolf von der Uni Genf. Mit einer speziellen Röntgenquelle gelang es den Forschern, die ersten, extrem schnell ablaufenden Schritte der lichtinduzierten Harnstoff-Umwandlung zu enträtseln.
Bei dem Versuch schoss das Team in Laboren der Uni Genf die Lichtpulse eines Lasers durch einen Strahl aus einer hochkonzentrierten Harnstoff-Lösung. Dabei ionisierten die Lichtblitze manche der Harnstoffmoleküle und schlugen jeweils ein Elektron aus ihnen heraus. Unmittelbar darauf schickten die Forscher einen ultrakurzen Blitz aus weicher Röntgenstrahlung hinterher. Dieser fungierte als Sonde und verriet im Detail, wie der Harnstoff auf das Herausschlagen des Elektrons reagierte. Dann wiederholte das Team den Versuch mehrmals und veränderte dabei systematisch den zeitlichen Abstand zwischen Laser- und Röntgenpuls.
Dadurch ließ sich der Ablauf des Geschehens präzise rekonstruieren – bis auf wenige Femtosekunden genau. Eine besondere Herausforderung bestand darin, die gemessenen Spektren zu interpretieren. „Dazu bedurfte es detaillierter Computersimulationen, die wir am DESY in jahrelanger Arbeit entwickelt haben“, erläutert Ludger Inhester vom Center for Free-Electron Laser Science, einer gemeinsamen Einrichtung von DESY, Uni Hamburg und der Max-Planck-Gesellschaft.
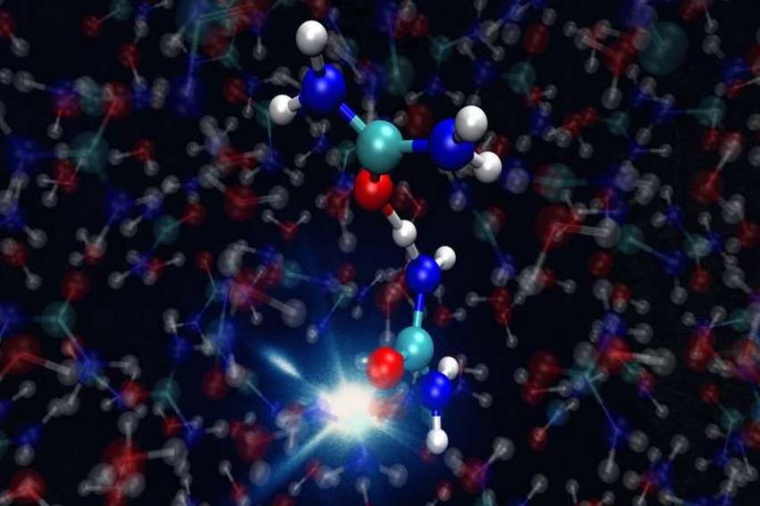
Mit diesem Setup konnte das Team die ersten Schritte der Harnstoff-Umwandlung enträtseln: Wird ein Harnstoffmolekül ionisiert, verliert es ein Elektron und ist elektrisch positiv geladen. Diese positive Ladung würde es liebend gern wieder loswerden. Möglich wird das, wenn sich ein anderes, nichtionisiertes Harnstoffmolekül in unmittelbarer Nähe befindet. „Dann schiebt das erste Molekül ein Proton, also einen Wasserstoffkern, zum neutralen Molekül hinüber“, erläutert Inhester. „Durch diesen Protonentransfer entsteht ein Harnstoff-Radikal sowie ein positiv geladenes Harnstoff-Ion.“ Beide sind chemisch reaktiv und könnten vor Jahrmilliarden zur Entstehung von RNA-Molekülen geführt haben – essentiellen Bausteinen des frühen Lebens. Mit dem Experiment konnte das Team nicht nur erstmals den rasanten „Protonen-Deal“ zwischen zwei Harnstoffmolekülen nachweisen, sondern auch seine Dauer bestimmen – der Prozess nimmt nur wenige hundert Femtosekunden in Anspruch.
„Das Neue an unserem Experiment ist, dass wir extrem schnelle Prozesse bei einem Molekül beobachten konnten, das in einer wässrigen Umgebung vorliegt“, betont Inhester. „Frühere Versuche hatten sich solche Reaktionen nur in der Gasphase angeschaut.“ Das Verhalten von Molekülen, die in einer Flüssigkeit wie Wasser schwimmen, ist für viele Fragestellungen besonders relevant – insbesondere für biologische Prozesse. Experimente in einer solchen Umgebung bilden nicht nur für die Messtechnik eine Herausforderung, sondern auch für die Computerberechnungen, die zur Interpretation der Messdaten nötig sind.
Künftig könnte die neue Methode verraten, was im Detail passiert, wenn ionisierende Strahlung auf Gewebe trifft und dort Strahlenschäden verursacht. Ferner liebäugeln die Forscher damit, ähnliche Experimente auch an einer sehr viel größeren Röntgenquelle zu machen – dem europäischen Röntgenlaser European XFEL in Hamburg. Die gut drei Kilometer lange Anlage, an der DESY maßgeblich beteiligt ist, liefert die stärksten Röntgenblitze der Welt. „Auf diese Weise könnten wir den Protonentransfer aus anderen Blickwinkeln untersuchen“, sagt Inhester – und hofft, dadurch weitere Einzelheiten über diesen sehr fundamentalen Prozess herauszufinden.
DESY / RK
Weitere Infos
- Originalveröffentlichung
Z. Yin et al.: Femtosecond Proton Transfer in Urea Solutions Probed by X-ray Spectroscopy, Nature, online 28. Juni 2023; DOI: 10.1038/s41586-023-06182-6 - Laboratorium für physikalische Chemie, Eidgenössische Technische Hochschule Zürich, Schweiz
- GAP-Biophotonics, Université de Genève, Genf, Schweiz
- CFEL – Center for Free-Electron Laser Science CFEL, Deutsches Elektronen-Synchrotron, Hamburg











