Wundheilung mit Oberflächenwellen
Sanfte Aktivierung regt Wundheilung und Zellmigration merklich an.
Eine Entdeckung von Wissenschaftlern der Universität Augsburg hat das Potenzial, die Wundheilung zu beschleunigen. Durch akustische Oberflächenwellen bringen sie unter Laborbedingungen Zellen in Bewegung und regen das Zellwachstum an, wodurch sich Wunden schneller schließen. Die angeregte Zellmigration lässt sich sogar auf 130 bis 140 Prozent steigern. „Ein weiterer Durchbruch ist, dass wir den Effekt auch bei anderen Gewebezellen wie beispielsweise Nierenzellen nachweisen konnten. Das ist ein Indikator dafür, dass der Effekt durchaus universell sein könnte“, meint der Biophysiker Christoph Westerhausen.
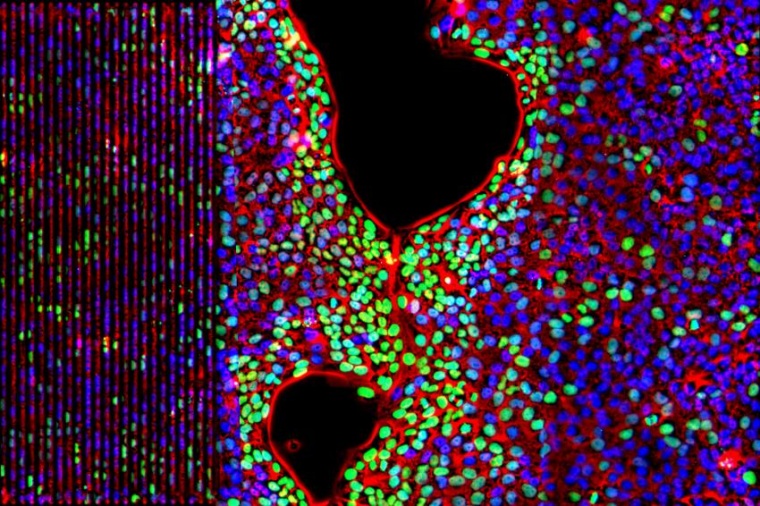
Auf einem Chip legen die Forscher an Elektrodenstrukturen eine elektrische Wechselspannung an. Dadurch entsteht ein elektrisches Feld, das dazu führt, dass sich die Atome des Chips nahe der Oberfläche gegeneinander verschieben – es entsteht eine Wellenbewegung auf der Oberfläche. Diese durch ein Hochfrequenzsignal erzeugten „Nano-Beben“ lösen eine interessante Wechselwirkung mit den darauf sitzenden Zellen aus. Bei einer kontinuierlichen „Beschallung“ einer künstlichen Wunde steigt die Geschwindigkeit, mit der sich die Zellen bewegen, um bis zu 150 Prozent. Dies beschleunigt das Verschließen einer Wunde signifikant im Vergleich zu Stellen, die nicht beschallt werden.
Die Wellen bewegen sich mit einer Geschwindigkeit von 14.000 Kilometern pro Stunde und dringen dabei doch nur eine halbe Wellenlänge in das Zellmaterial ein. „Bei dieser Methode werden die Zellen mit den Schallwellen nur leicht ‚gekitzelt‘ und nicht mit Gewalt verschoben. Wir arbeiten hier also mit leisen und sanften Wellen“, sagt Westerhausen. Was den Biophysiker sehr freut, ist, dass in den letzten Jahren zu dieser Forschung neben dem Erstautor Manuel Brugger, der sich in seiner Doktorarbeit mit dem Thema beschäftigt hat, viele Studierende im Rahmen von Abschlussarbeiten beigetragen haben, was in eine Mitautorenschaft mündete.
„Die mechanische Bewegung der Welle wird auch durch ein sich mitbewegendes elektrisches Feld begleitet. In unserer neueren Forschung hat sich gezeigt, dass es mit großer Wahrscheinlichkeit die mechanische Komponente des Nano-Bebens ist, die dazu führt, dass die Zellen sich schneller Richtung Wunde bewegen. Das elektrische Feld, das ebenfalls erzeugt wird, spielt dafür eine untergeordnete Rolle“, so Westerhausen. Die Frage, wie sich der Effekt weiter erklären lässt, treibt die Forscher aber weiter an. Daher hat das biophysikalische Forschungsteam mit dem Lehrstuhl für Biochemie von Regina Fluhrer an der Medizinischen Fakultät zusammengearbeitet, um besser zu verstehen, welche biochemischen Prozesse dabei ablaufen. So lässt sich auch die Rolle der Zellmembran untersuchen. „Künftig wollen wir gezielt die Adhäsionseigenschaft der Zellen modifizieren, also wie gut sie auf dem Chip haften“, erklärt Westerhausen.
Eine weitere Erkenntnis der gemeinsamen Zusammenarbeit zwischen Biophysik und Biochemie zeigt, dass die Stimulation bei den Zellen nicht zu einem erhöhten Stresslevel führt. Denn chemische wie mechanische Einwirkungen oder andere Umwelteinflüsse können in Zellen zu erhöhtem Stress führen, der sich darin zeigt, dass sich Sauerstoffradikale bilden. Bei der Beschallung mit akustischen Oberflächenwellen zeigten die Zellen keine solche Reaktion. Hier zeige sich auch, so Westerhausen, dass bei der Methode die Zellen nur sanft angeregt werden. „Wir kitzeln die Zellen nicht so stark, bis sie sich vor Lachen krümmen.“
Aktuell findet die Grundlagenforschung unter Laborbedingungen statt. Anwendungsmöglichkeiten für die Technologie gäbe es viele. Der Chip, der die akustischen Oberflächenwellen erzeugt, könnte in Form eines biegsamen Materials hergestellt werden und etwa in einem Pflaster die Wundheilung beschleunigen. Oder bei einer Hüft-OP könnte das Implantat entsprechend beschichtet werden, sodass der integrierte Chip von außen mit Energie versorgt werden könnte – wie bei RFID-Chips – und die Wundheilung nach dem Eingriff beschleunigen wird. „Das sind nur einige Szenarien, die vorstellbar sind“, so Westerhausen, „aber noch in der Zukunft liegen.“
Aber auch intrazelluläre Mechanismen hat das Forschungsteam im Blick. Da sich die Migration von Zellen durch die „Nano-Beben“ beeinflussen lässt, könnten auch andere Prozesse stimuliert werden wie die Art und Weise, wie Zellen Stoffe in sich aufnehmen. Ein Einsatzgebiet bietet sich bei der Entwicklung von Medikamenten, spezieller bei der Suche nach neuartigen Wirkstoffen. Denn es gibt Wirkstoffe, die von den Zellen nicht über die Zellmembran aufgenommen werden. „Bei der Frage, was ein bestimmter Stoff in der Zelle selbst bewirken könnte, wenn er dort hineinkäme, kann unsere Forschung möglicherweise helfen“, so Westerhausen. Inwiefern die akustischen Oberflächenwellen die Zellhülle vorübergehend durchlässig machen können, erforschen die Wissenschaftler gemeinsam mit Pharmazeuten der LMU in München. Für dabei identifizierte neue Wirkstoffe könne anschließend eine geeignete Hülle entwickelt werden, damit dieser dann als Medikament leichter die Zellmembran durchqueren kann.
Die Erforschung und vielfältige Anwendung des Umstandes, dass sich Schallwellen wie „Nano-Beben“ an der Oberfläche eines Kristalls ausbreiten, wenn ein passendes Hochfrequenzsignal angelegt wird, gilt seit vielen Jahren bereits als international anerkannte Spezialität des Augsburger Lehrstuhls für Experimentalphysik I (Achim Wixforth). Sie wird in verschiedenen Kontexten – wie beispielsweise der Wundheilung – genauer erforscht.
U. Augsburg / DE











